
·“我们的这个发现可以指导临床上所有 CAR 的优化,我们可以告诉你一个 CAR 有没有基底信号,有的话是多少,它的基底信号是否处在最优范围,不是的话又该如何优化。这对于每一个特异性治疗都非常重要。”
研究成果简介。视频来源:复旦大学附属眼耳鼻喉科医院(02:22)
CAR-T 细胞耗竭一直是困扰 CAR-T 疗法的难题。
3 月 8 日,上海科技大学生命科学与技术学院王皞鹏课题组与复旦大学附属眼耳鼻喉科医院吴海涛团队、中科院分子细胞科学卓越创新中心许琛琦实验室,以及上海市第一人民医院宋献民课题组合作在国际著名期刊《细胞研究》(Cell Research)(影响因子:46)上发表了题为《调节嵌合抗原受体(CAR)的电荷密度可优化基底信号传导和 CAR-T 细胞适应性》(Tuning Charge Density of Chimeric Antigen Receptor Optimizes Tonic Signaling and CAR-T Cell Fitness)的研究论文。该研究成功解析了基底信号(Tonic signaling)形成的机制——CAR 胞外区域表面带正电荷的斑块(PCPs)介导 CAR 自发聚集,从而产生基底信号。据此,研究团队提出了两种新的优化 CAR 的思路:在体外 CAR-T 扩增期间提高培养基中的钠盐离子浓度,或基因改造引入改变 PCPs 的突变。
论文截图。
据称,这一发现可显著缓解 CAR-T 细胞耗竭,进而提高 CAR-T 治疗实体肿瘤的效果。“我们的这个发现可以指导临床上所有 CAR 的优化,我们可以告诉你一个 CAR 有没有基底信号,有的话是多少,它的基底信号是否处在最优范围,不是的话又该如何优化。这对于每一个特异性治疗都非常重要。”3 月 6 日,王皞鹏教授接受澎湃科技专访时解释。
王皞鹏教授是上海科技大学生命科学与技术学院的免疫学专家,研究方向聚焦于T细胞功能的调控机制,探索肿瘤免疫疗法的新靶点,开发新型T细胞免疫疗法。王皞鹏的博士后导师是 20 世纪 90 年代初 CAR-T 的发明者之一、美国加州大学旧金山分校(University of California, San Francisco)的亚瑟·韦斯(Arthur Weiss)院士。在他的实验室里,王皞鹏开始研究T细胞免疫疗法,2015 年回国后,王皞鹏一直致力于 CAR-T 疗法的研发。
CAR-T 的困境
CAR-T,即嵌合抗原受体T细胞(Chimeric Antigen Receptor T Cells),是一种细胞免疫疗法。其具体操作过程是:先由医疗机构采集患者的外周血淋巴细胞,再送往药企或实验室,通过基因修饰技术将T细胞改造为可以识别并杀死相应肿瘤细胞的 CAR-T,经过扩增生产后将 CAR-T 细胞通过静脉输液方式重新输回患者体内。
王皞鹏介绍,目前,CAR-T 疗法面临四个困境。“一是 CAR-T 在实体肿瘤的治疗中举步维艰,因为实体肿瘤是一个固态的相对封闭的空间,CAR-T 细胞很难进入。二是,实体肿瘤异质性显著。血液肿瘤往往都带有一个标记物,CAR-T 细胞可以通过这个标记物很好地感知肿瘤,但是实体肿瘤很难找到一个单一的标记物。更麻烦的是,同一个肿瘤里可能有一部分表达标记物A,另一部分表达标记物B,因此,CAR-T 细胞很难精准地同时感知所有实体肿瘤细胞。三是 CAR-T 细胞在体内持续时间不够长,这是导致肿瘤复发的一个重要因素。四是 CAR-T 细胞耗竭,就像人不停地去干同一件事情,他的耐心和精力会耗尽一样,T细胞不停地重复识别同一个信号和杀死的动作,它就会进入耗竭状态。”
“如果把这四个问题都解决,CAR-T 临床上的两个难题——血液肿瘤的复发和实体肿瘤的低效,都可以随之解决。” 王皞鹏说。
基底信号传导可以定义为不依赖于抗原的 CAR-T 细胞活化。“CAR-T 细胞在没有肿瘤抗原刺激的情况下,也会释放微弱的、持续不断的信号,它可以让细胞在体内存活的时间比较长。”王皞鹏解释,“可以把 CAR-T 细胞想象成一辆车,如果总是不启动,它就容易坏,要时不时启动一下,它的元件才能保持活性。基底信号就是起到这种怠速作用。我们这次研究的问题就是——‘怠速’形式对于 CAR-T 来说是不是必要的。”
2015 年,美国国立卫生研究院国家癌症研究所(National Cancer Institute,National Institutes of Health)的一项研究发现,高基底信号会导致 CAR-T 细胞自发进入耗竭状态。研究人员将两种不同基底信号的 CAR——一种是基底信号较弱,常用于血液肿瘤的 CD19.28z;另一种是基底信号较强,常用于胶质瘤的 GD2.28z,表达在细胞膜上,将 CAR 和荧光蛋白融合后发现,CD19.28z CARs 均匀分布在T细胞表面而 GD2.28z CARs 则形成聚集。当研究人员将这两种 CAR 注入肿瘤模型时,发现弱基底信号的 CAR-T 可以抑制肿瘤,高基底信号的 CAR-T 则不起作用。
抑制基底信号一度成为业内的共识。然而,2021 年,美国宾夕法尼亚大学(the University of Pennsylvania)的一项研究得出一个截然相反的结论——高基底信号可增强某些 CAR-T 细胞的临床疗效。
“所以这个领域里一直有两个没能解决的问题,一是基底信号是如何形成的,二是基底信号到底是强好还是弱好。”王皞鹏说。
王皞鹏他们就想解决这两个问题。
解析基底信号的机制
王皞鹏团队首先定量了基底信号的大小——他们制定了一个“基底信号指数”,“我们把 CAR 放在一个T细胞株上,如果产生信号,激活标记物(marker)会上调。标记物上调越多,说明基底信号越强,标记物越少,说明基底信号越弱。我们首先观察了临床上常用的三种 CAR,发现标记物和基底信号指数呈正相关,证明我们的模型可用。”王皞鹏解释。
随后,他们用这个细胞系定义了临床上常见的十种 CAR,产生了三点发现:第一,在他们的实验中,观察的所有 CAR 都有基底信号;第二,基底信号强弱的范围非常大;第三,临床上用于血液肿瘤效果比较好的 CAR,基底信号较弱,而用于实体肿瘤的 CAR 效果较差,基底信号较强。“我们猜想,CAR-T 在实体肿瘤中效果不好,很可能是因为基底信号太强,如果减弱它的基底信号,很可能会推进 CAR-T 在实体肿瘤上的治疗。”王皞鹏说。
CAR-T 在实体肿瘤中疗效有限,T细胞耗竭是一个很重要的原因。过往的研究表明,高基底信号会导致T细胞耗竭。为了对这一发现进行验证,王皞鹏团队定义一个耗竭指数(exhaustion score)对每种 CAR-T 的耗竭程度进行打分,发现基底信号越高的 CAR-T 细胞越容易耗竭。
在此基础上,他们开始探究是什么引发了基底信号。T细胞受体前体(pre-TCR)已经被发现具有很强的基底信号。过去有研究者在其表面做了突变,发现只要消除正电荷,基底信号就会消失,而重新引入正电荷,基底信号也会重新出现。同样的现象也出现在B细胞受体前体(pre-BCR)中。这说明,蛋白表面的正电荷在基底信号的形成中起作用。
这启发了王皞鹏团队:不同的 CAR 表面的电荷会不会不同?为了找到这个问题的答案,他们把 CAR 的正、负电荷标都进行了标记,观察发现,基底信号弱的 CAR 正负电荷均匀分布在蛋白表面,而基底信号强的 CAR 的正电荷会聚集在一起,形成一个斑块。接着,他们开发了 PCP 评分来量化正电荷斑块的大小,作为基底信号的预测因子。计算后发现,斑块面积越大,基底信号越强。据此,王皞鹏团队猜想,正电荷的斑块是让 CAR 聚集的动力。后续研究发现,产生最佳基底信号的 PCP 评分可能在 46-56 分左右。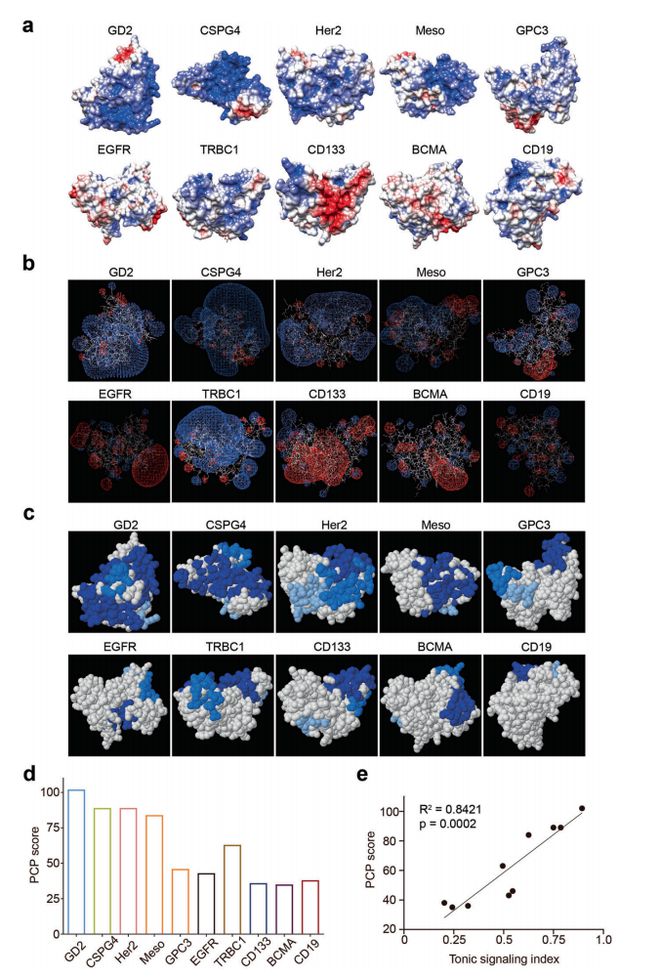
CAR 胞外区域表面带正电荷的斑块(PCPs)引发基底信号的产生。图片来源:王皞鹏团队论文
两种优化 CAR 的策略
王皞鹏团队使用了两种方法来验证静电作用对基底信号的影响。第一种是在培养基中加入盐,盐会包裹电荷,让 CAR 的正电荷的表面带有负电荷的氯离子,从而屏蔽了电荷之间的相互作用。他们观察后发现,在加入盐后,基底信号较高的 CAR 开始在细胞膜上均匀分布,不再形成聚集,基底信号指数下降,CAR-T 细胞对肿瘤的杀伤力也提高了一倍。“所以我们认为,在培养容易耗竭的 CAR-T 时,提高盐浓度,将盐浓度调控到最优,可以增强 CAR-T 的功能。”王皞鹏说。
王皞鹏向澎湃科技表示,在培养基中加入盐的方法有很强的可操作性,因为盐(氯化钠)没有毒性,而且培养基中本身也有盐,只需调整它的浓度即可,最大的问题是找到盐的最优浓度。他也坦言,这并不是“治本”的方法,“培养过程中,在盐的保护下,T细胞不耗竭,但在输入患者体内时,T细胞仍有可能回到耗竭的状态。”
他认为能够“治本”的方法是第二种——通过基因改造减小 CAR 表面的正电荷斑块。“我们慢慢地把斑块打散,发现基底信号指数和耗竭指数都下降了,对肿瘤的杀伤力也提高了。”王皞鹏说。
王皞鹏团队的最后一步是反证。他们使用在临床上治疗血液肿瘤效果很好的 CD19.CAR,希望通过提高它的基底信号,来观察它的耗竭指数。然而结果和他们的假设相反,在提高了 CD19.CAR 的基底信号之后,它的功能加强了,更好地清除了肿瘤。这给了王皞鹏团队另一个启发:基底信号并不是越低越好。“基底信号和 CAR-T 疗效之间的关系是峰形的,最优值在中间,而不是两端。如果基底信号太低,就没有力量驱动 CAR-T 保持怠速活动,导致其持久性不足,如果基底信号太高,它就会驱动 CAR-T‘狂奔’快速地进入耗竭状态。”王皞鹏解释。
“这种方法在体内和体外都可行,技术层面上不难,但需要能够测量基底信号的体系。相比加盐,这种方法的前期研发成本更高,但带来的收益也相对更高。”王皞鹏向澎湃科技透露,他们计划把这个体系做成一个网站,只要输入 CAR 序列,网站就可以给出调控基底信号基因改造的方案,使整个过程更加便捷与自动化。
王皞鹏团队一直致力于优化 CAR 的设计。此前,他们通过研究 CAR 受体在 CAR-T 细胞中转运、降解的调控机制,设计了一种可循环 CAR,提高了 CAR-T 在体内的持续能力,相关成果于 2020 年 8 月发表于国际顶级期刊《免疫学》(Immunity)。“这是另外一个优化 CAR 的维度,也就是改变 CAR 受体蛋白的寿命。”王皞鹏告诉澎湃科技,接下来他们还会继续从不同的维度去进行 CAR 的优化,“我们希望手上有很多不同维度的‘武器’,看看能否通过某一个维度的优化,或通过不同维度优化的组合,产生一个最优的 CAR。”






